「抗体」の開発には、従来、膨大な時間とコストがかかっていました。しかし今、AI(人工知能)の力でこのプロセスを効率化する技術が、中国で特許として成立しています。
本記事では、中国特許 CN 118658515 B「抗体構造の微調整に基づくタンパク質大規模言語モデルを用いて、特定の抗原に対する新しい抗体を設計するシステム」について、専門家でない方にもわかるように解説します。
発明の概要:AIを「抗体の専門家」に育てる
この特許は、タンパク質の大規模言語モデル(いわば「AIの脳」)を、抗体という特殊なタンパク質に特化して教育し、新しい抗体を自動設計するシステムに関する発明です。
技術分野としては、人工知能(ディープラーニングや機械学習)とバイオテクノロジー(抗体医薬品の研究開発)が交差する領域に位置しています。
解決しようとしている2つの課題
課題1:従来の実験手法はコストが高い
従来の抗体開発では、抗体ライブラリを構築し、人工的にアミノ酸を変異させてからファージディスプレイ技術などの実験的手段でスクリーニングを行うのが一般的でした。しかし、この方法は非常に時間がかかり、ランダム性が高く、効率の悪さが問題でした。
課題2:既存のAI技術は「抗体の専門家」ではなかった
近年、深層学習を用いたタンパク質の配列最適化技術が発展していますが、既存のモデルの多くは一般的な広範なタンパク質配列に基づいて訓練されたものでした。抗体という特殊な構造を持つタンパク質の設計に特化した統合的なプロセスは、確立されていませんでした。
技術的特徴:5つのモジュールが連携する統合システム
この発明のアプローチは、一般的なタンパク質言語モデル(ESM-2など)に抗体の構造・配列データベース(SAbDab、SKEMPI_V2、OASなど)を学習させて「抗体専用のモデル」を構築し、以下のモジュールを連携させることで課題を解決します。
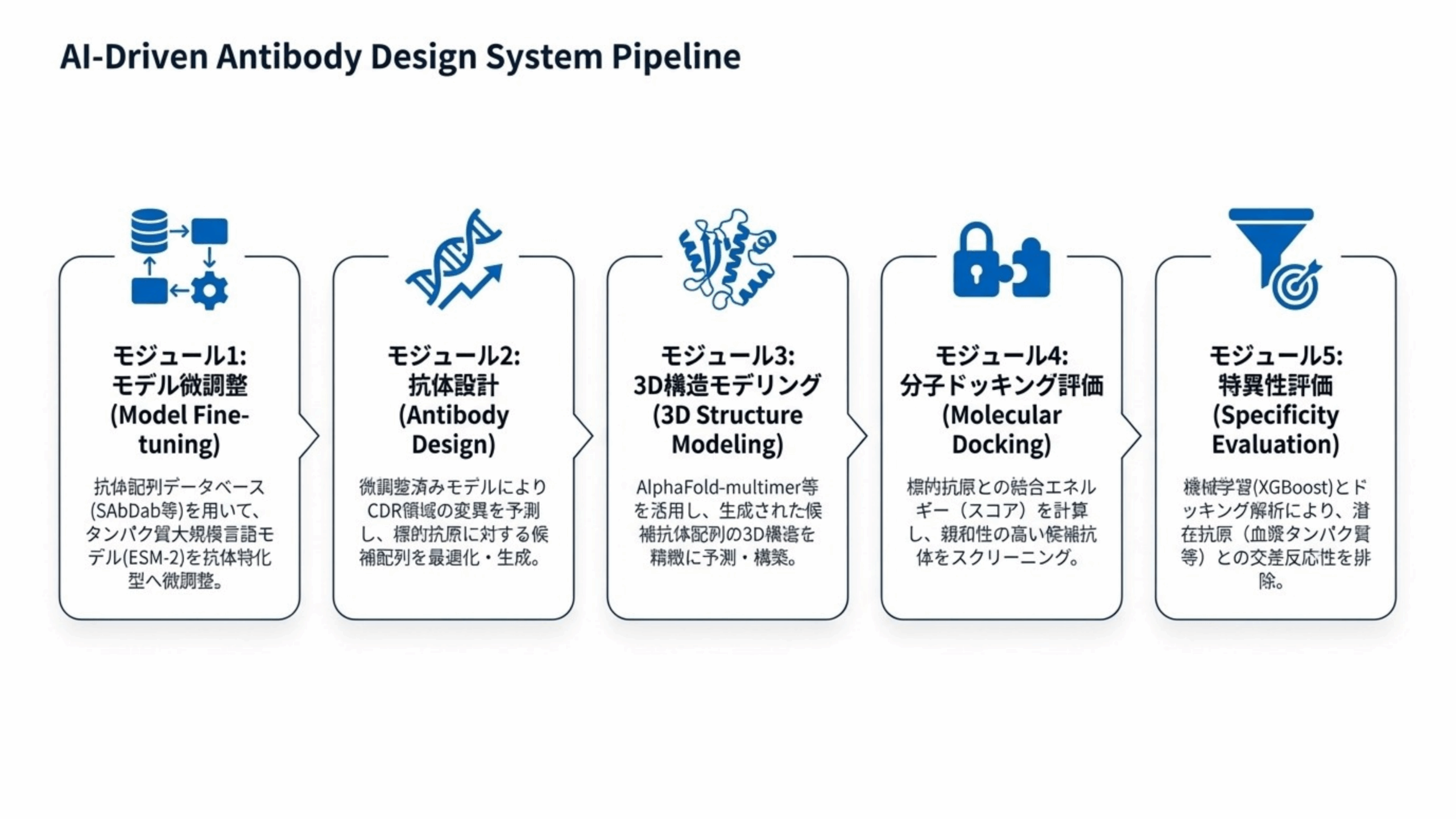
モジュール1:モデル微調整(AIを抗体の専門家に育てる)
一般的なタンパク質を理解している大元のAI(ESM-2モデル)を、抗体専用のAIへと教育します。抗体データベースを教材として読み込ませ、抗体の配列の中からわざと一部を隠して「ここには何が入るか?」という穴埋めクイズを繰り返すことで、AIに抗体のルールを深く理解させます。
モジュール2:抗体設計(より良い設計図を提案する)
専門家になったAIが、実際に抗体の性能をアップグレードさせる設計図を作ります。抗体全体ではなく、病気(抗原)と直接結合する一番重要な「手」の部分(CDR:相補性決定領域)をピンポイントで改良します。
モジュール3:3D構造モデリング(設計図を立体にする)
ノーベル賞受賞AIプログラム(AlphaFold-multimer)などを使って、設計図を空間的な3Dモデルに組み立てます。5回以上予測を行い、最も安定した形を採用します。
モジュール4:分子ドッキング評価(パズルの相性をテストする)
3Dになった抗体が抗原(ターゲット)にパズルのようにピッタリ強力に結合するかをシミュレーションします。
モジュール5:安全性チェック(副作用リスクを排除する)
最後に機械学習(XGBoost)を使い、血液中にある正常な成分等に間違って結合しないか(特異性)をチェックし、安全な抗体を最終的に選び抜きます。
実験で証明された効果:AIが設計した抗体は本当に使えるのか?
この特許では、AIシステムの有効性を「コンピューター上のシミュレーション」だけでなく、実際の実験室での生化学的検証(wet実験)でも確認しています。明細書の「実施例2:新抗体の検証」に記載された結果は、この発明の実用性を強く裏付けるものです。
実験の概要
元の抗体(抗体O)と、本特許のAIシステムによって最適化・設計された3つの新しい抗体「LC166」「LC167」「LC168」を比較しました。各抗体は血清に添加され、2000倍希釈から段階的に希釈してテストが行われています。
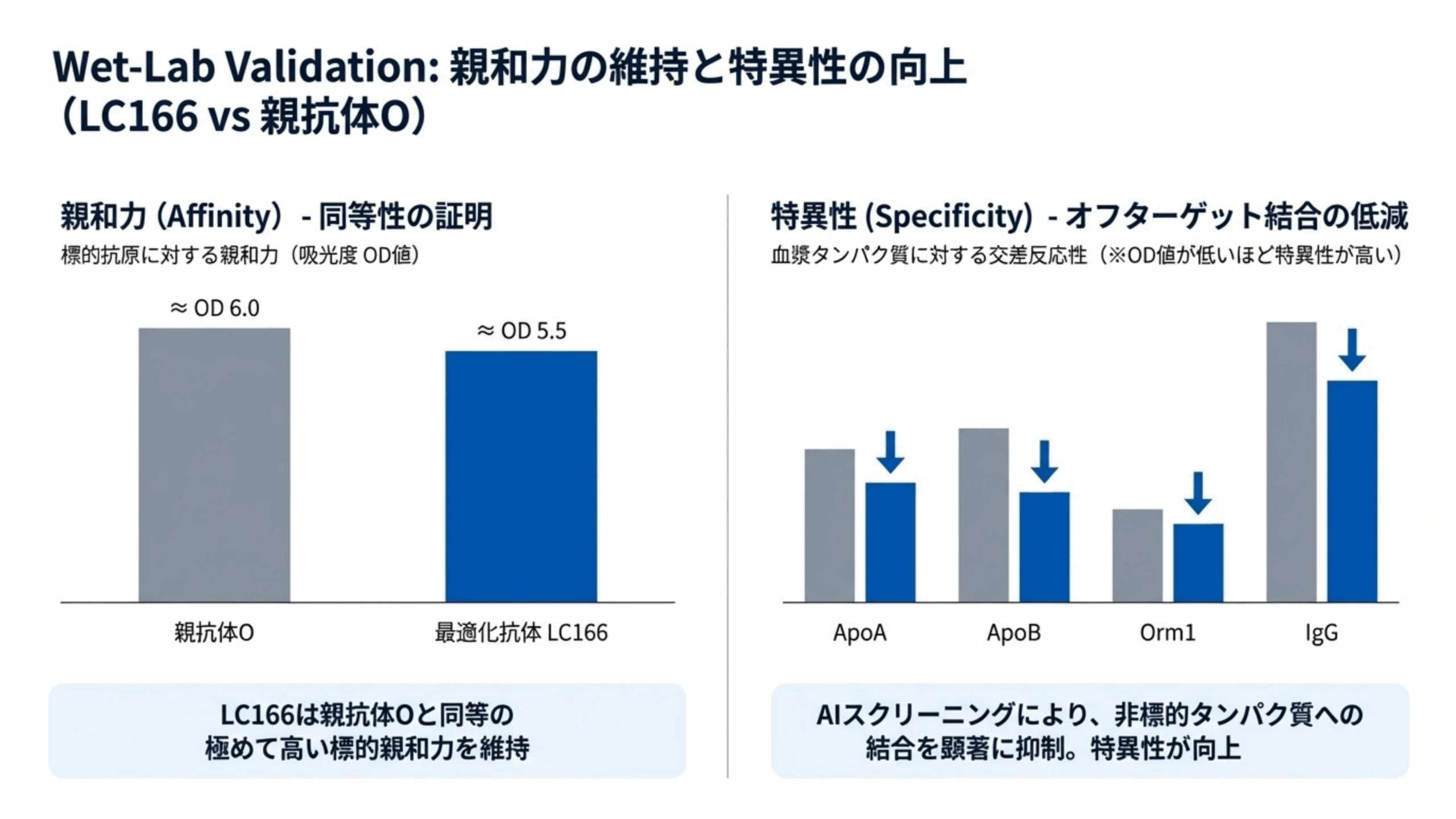
結果1:ターゲットへの結合力(親和力)
抗体がどれだけ強くターゲット(病気の原因となるタンパク質)にくっつくかを調べた結果、AIが設計した新抗体「LC166」は、元の抗体Oに近いレベルの親和力を維持していることがグラフ(図4)から確認されました。
つまり、AIが設計した抗体でも、元の抗体とほぼ同じ「強さ」で病気のターゲットを捕まえることができるということです。
結果2:安全性(特異性)の大幅な向上
さらに重要なのが、特異性(正常なタンパク質に間違ってくっつかないか)の検証結果です。血漿中に多く存在する正常なタンパク質4種類(ApoA、ApoB、Orm1、IgG)に対するテストが行われました。
- ApoA・ApoBに対して:新抗体「LC166」「LC167」は、元の抗体Oよりも明らかに結合力が弱い(=誤って結合しにくい)
- Orm1・IgGに対して:新抗体「LC166」は、元の抗体Oよりも結合力が弱い(=副作用リスクが低い)
実験結果のまとめ
この実験で最も注目すべき成果は、AIが設計した「LC166」は、元の抗体とほぼ同等のターゲット結合力を維持しながら、正常な血液タンパク質への誤結合が減少したという点です。言い換えれば、「狙ったものにはしっかりくっつくが、狙っていないものにはくっつきにくい」という、抗体医薬品にとって理想的な性質をAIが実現したことになります。
この結果は、本特許のAIシステムが単にコンピューター上のシミュレーションにとどまらず、AIが設計した抗体(LC166)が元の抗体と同等の結合力を維持しながら特異性を向上させたことを実証しています。
まとめ
中国特許 CN 118230822 Bは、AIの言語モデル技術を抗体医薬品の設計に応用した発明です。5つのモジュールが連携する統合システムにより、抗体開発のプロセスを短縮できる可能性があります。
さらに、実験室でのwet実験により、AIが設計した抗体(LC166)が元の抗体と同等の結合力を維持しながら特異性を向上させたことが実証されています。
なお、本特許は審査では、拒絶理由を通知されず、出願からわずか約6ヶ月という非常に短期間で、2024年12月6日に特許権が付与されました。この迅速な権利化は、本発明の新規性・進歩性が審査官に高く評価されたことを示すものと言えます。
